Last Updated on 14 มีนาคม 2024 by นพ.ประสิทธิ์ วิริยะกิจไพบูลย์
เนื้อหาในเอกสาร
1. มะเร็งที่ถ่ายทอดทางพันธุกรรม
มะเร็งที่พบในผู้ป่วยถูกแบ่งออกเป็น 2 ประเภท ได้แก่ มะเร็งที่เกิดขึ้นเองในบุคคลนั้น ๆ (Sporadic cancers) และมะเร็งที่เกิดจากการถ่ายทอดทางพันธุกรรม (Hereditary cancer) ที่มีสาเหตุหลักมาจากการกลายพันธุ์ของยีนสืบทอดต่อกันมาตั้งแต่บรรพบุรุษ
มะเร็งที่เกิดจากการถ่ายทอดทางพันธุกรรมนี้ พบว่าประชากร 3 ใน 1000 คน จะได้รับการถ่ายทอดยีนกลายพันธุ์ที่เกี่ยวข้องกับมะเร็ง ซึ่งประชากรกลุ่มนี้มีความเสี่ยงต่อการเป็นมะเร็งมากกว่าผู้ที่ไม่ได้รับการถ่ายทอดทางพันธุกรรม ตัวอย่างเช่น BRCA1 และ BRCA2 เป็นยีนที่มีความเกี่ยวข้องกับมะเร็งเต้านมและมะเร็งรังไข่ โดยพบว่าผู้ที่ได้รับการถ่ายทอดทางพันธุกรรมมา มีความเสี่ยงในการเกิดมะเร็งมากกว่าผู้ที่ไม่ได้รับการถ่ายทอดทางพันธุกรรม มากถึง 75% ดังนั้นการตรวจคัดกรองมะเร็งที่ถ่ายทอดทางพันธุกรรมจึงมีความสำคัญยิ่งในผู้ที่ประวัติมะเร็งในครอบครัว หรือ ผู้ที่ต้องการหาความเสี่ยงของมะเร็งที่ถ่ายทอดทางพันธุกรรม
2. ขั้นตอนการเก็บสิ่งส่งตรวจ
2.1. ก่อนเก็บสิ่งส่งตรวจสิ่งที่ต้องเตรียม
2.1.1. กรอกเอกสารขอตรวจ
แพทย์ผู้ส่งตรวจต้องกรอกเอกสารขอตรวจเพื่อคัดกรองหายีนมะเร็งที่ถ่ายทอดทางพันธุกรรมอย่างครบถ้วน ชัดเจน และเป็นความจริง พร้อมกับลงนามในคำยินยอมของแพทย์ ส่วนผู้รับบริการอ่านและลงนามในเอกสารความยินยอมในการตรวจ
2.1.2. ตรวจสอบข้อมูลในบัตรประชาชน
แพทย์ หรือ ผู้เชี่ยวชาญที่ให้บริการด้านสุขภาพ ต้องตรวจข้อมูลของผู้ป่วยและรายละเอียดอื่น ๆ เพื่อให้แน่ใจว่าข้อมูลในเอกสารขอตรวจถูกต้อง
2.1.3 กรอกเอกสารยินยอมการส่งตรวจ
แพทย์ หรือ ผู้เชี่ยวชาญที่ให้บริการด้านสุขภาพต้องอธิบายรายละเอียดการตรวจคัดกรองพันธุกรรมให้ครบถ้วนแก่ผู้รับบริการ และสมาชิกในครอบครัว/ผู้ปกครองของผู้รับบริการ โดยอธิบายความสำคัญ ข้อจำกัด ความเสี่ยง และประโยชน์ของการตรวจคัดกรองมะเร็งที่ถ่ายทอดทางพันธุกรรม รวมถึงผู้รับบริการต้องได้รับการอธิบายเกี่ยวกับขั้นตอนการทดสอบอย่างถูกต้องและครบถ้วน จากนั้นผู้รับบริการหรือผู้ปกครองต้องลงนามให้ความยินยอมก่อนทำการตรวจคัดกรองหายีนมะเร็งที่ถ่ายทอดทางพันธุกรรม
2.1.4. การบ่งชี้สิ่งส่งตรวจ
สิ่งส่งตรวจต้องแสดงข้อมูลที่ถูกต้องและชัดเจน โดยต้องแสดงข้อมูล ชื่อผู้รับบริการ และอายุบนหลอดเก็บเลือด ฉลากที่ใช้อาจเป็นบาร์โค้ดจากทางโรงพยาบาลหรือสถานพยาบาล ควรติดบาร์โค้ดในแนวนอนกับหลอดเก็บเลือดเพื่อให้สะดวกต่อการอ่านข้อความในฉลากได้อย่างชัดเจน และหลีกเลี่ยงการปิดทับขีดบอกปริมาตรเลือดในหลอดเลือด
2.2. ชนิดของสิ่งส่งตรวจ มี 2 ชนิด คือ เลือด และ ดีเอ็นเอ รายละเอียดดังนี้
2.2.1. เลือดจากหลอดเลือดดำ
2.2.1.1. ชนิดของหลอดเก็บเลือดที่ใช้
ใช้หลอดเก็บตัวอย่างเลือดทางคลินิกชนิด EDTA (ฝาสีม่วง) ปริมาตร 3 มล. จำนวน 1 หลอด ห้ามใช้หลอดเก็บเลือดชนิดอื่น ๆ เก็บสิ่งส่งตรวจ
2.2.1.2. ขั้นตอนการเก็บเลือด
ทำการเจาะเลือดจากหลอดเลือดดำด้วยการใช้ syringe อย่างน้อย 3 มล. โดยบรรจุเลือดลงหลอดเก็บเลือดชนิด EDTA ขนาด 3 มล. โดยให้ใช้เข็มขนาดใหญ่กว่าเบอร์ 21G ขึ้นไป เพื่อป้องกันเม็ดเลือดแดงแตก หรือสามารถใช้หลอดเลือดแบบสูญญากาศได้ จากนั้นให้ผสมสารป้องกันเลือดแข็งตัวโดยการกลับหลอดเลือดอย่างเบามือจำนวน 8-10 ครั้ง
2.2.1.3. ลักษณะตัวอย่างที่เหมาะสมในการส่งตรวจ
ไม่พบการแข็งตัวของเลือด หรือ ภาวะเม็ดเลือดแดงแตก และการปนเปื้อนจุลชีพ
2.2.1.4. การขนส่งสิ่งส่งตรวจ
ก่อนการขนส่งตัวอย่าง เจ้าหน้าที่กรุณาตรวจสอบหลอดเลือดและเอกสารขอตรวจก่อนส่งตรวจ และจัดส่งตัวอย่างเลือดหลังจากเจาะเลือดภายใน 24 ชม. ที่อุณหภูมิ 4◦C (หากไม่สามารถจัดส่งตัวอย่างได้ ควรเก็บรักษาตัวอย่างเลือด ที่ 4◦C และจัดส่งภายใน 5 วันหลังจากวันที่เจาะเลือด)
2.2.2. ดีเอ็นเอ
2.2.2.1. การสกัดดีเอ็นเอ
ควรปฏิบัติตามขั้นตอนต่าง ๆ ในการสกัดดีเอ็นเอจากตัวอย่างเลือด โดยขั้นตอนละลายตะกอนดีเอ็นเอให้ละลายด้วยบัฟเฟอร์ TE หรือ ddH2O
2.2.2.2. คุณภาพดีเอ็นเอ
ความเข้มข้นของดีเอ็นเอไม่น้อยกว่า 30 ng/μl ปริมาณดีเอ็นเอทั้งหมดไม่น้อยกว่า 3 μg และความบริสุทธิ์ ชนิด OD260/280 ควรอยู่ระหว่าง 1.8-2.0 และ ชนิด OD260/230 ควรอยู่ระหว่าง 2.0-2.2 ไม่ควรมีการสลายของสายดีเอ็นเอที่เห็นได้ชัด ซึ่งสามารถตรวจสอบได้โดยวิธีเจลอิเล็กโทรโฟรีซิส (Gel Electrophoresis) ดังรูปที่ 1 และไม่มีการปนเปื้อนสารพันธุกรรมชนิดอาร์เอ็นเอ โปรดแนบเอกสารผลการวัดคุณภาพดีเอ็นเอดังกล่าวในการจัดส่งตัวอย่างที่เป็นดีเอ็นเอมาด้วยทุกครั้ง
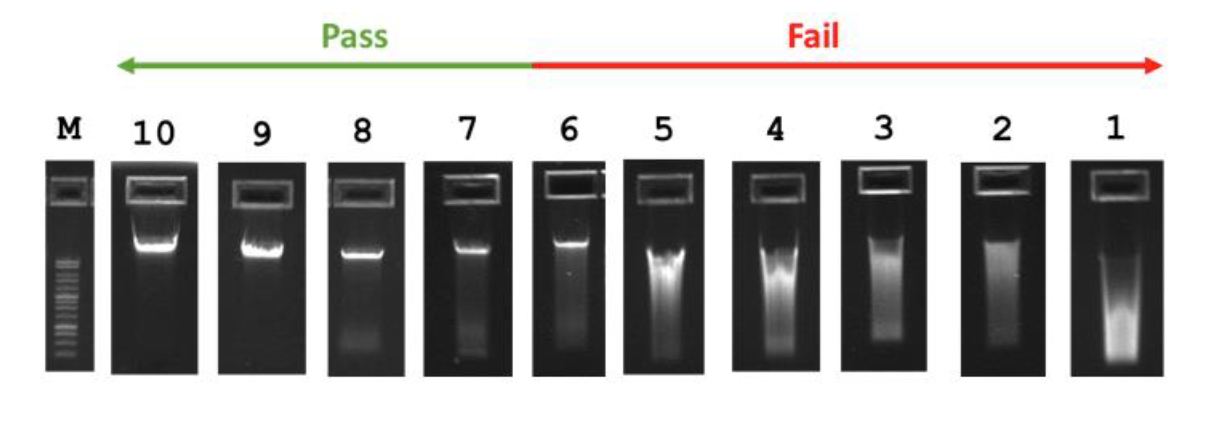
อ้างอิง: https://genomics.ed.ac.uk/resources/sample-requirements
รูปแสดงลักษณะเกณฑ์การรับตัวอย่างที่เป็นดีเอ็นเอ โดยจะสามารถส่งตรวจได้หากตัวอย่างมีลักษณะเป็นไปตามเลนที่ 7 ถึง 10 แต่หากมีลักษณะเป็นไปตามเลนที่ 1 ถึง 6 ซึ่งเป็นลักษณะของสายดีเอ็นเอที่ถูกทำลายอย่างเห็นได้ชัด จะไม่สามารถส่งตรวจได้
2.2.2.3. การขนส่งดีเอ็นเอ
ดีเอ็นเอที่สกัดใหม่หรือแช่แข็ง (เก็บไว้ที่ -20◦C ไม่เกิน 2 ปี และไม่ควรผ่านการละลายเกิน 5 ครั้ง) ก่อนส่งดีเอ็นเอควรตรวจสอบให้แน่ใจว่าไม่มีการปนเปื้อนตัวอย่าง และตัวอย่าง DNA ทุกหลอดมีข้อมูลที่ถูกต้อง และเตรียมน้ำแข็งแห้งให้เพียงพอจนกว่าสิ่งส่งตรวจมาถึงห้องปฏิบัติการ หากขนส่งทางไกล ควรใช้น้ำแข็งแห้ง 10-20 กก. แล้วแต่ระยะเวลาขนส่ง และควรใช้ภาชนะที่เหมาะสม เช่น กล่องโฟม และวัสดุกันกระแทก เพื่อหลีกเลี่ยงความเสียหายของสิ่งส่งตรวจ รวมถึงใช้ฉลากหรือป้ายที่เหมาะสมเพื่อระบุด้านบนและด้านล่างของภาชนะ
3. เกณฑ์การปฏิเสธสิ่งส่งตรวจ
3.1 เลือด
1) ข้อมูลที่ติดฉลากบนหลอดไม่สอดคล้องกับข้อมูลในเอกสารขอตรวจที่แนบมา ข้อมูลไม่สมบูรณ์ หรือข้อมูลไม่สามารถอ่านได้อย่างชัดเจน
2) ไม่มีเอกสารยินยอมการส่งตรวจ หรือ ข้อมูลไม่สมบูรณ์
3) หลอดเก็บเลือดที่มีการปนเปื้อน รอยแตก ฝาปิดหลวม หรือสถานการณ์อื่น ๆ ที่อาจนำไปสู่การรั่วไหลของสิ่งส่งตรวจ
4) ปริมาณเลือดน้อยกว่า 3 มล.
5) ได้รับตัวอย่างช้ากว่า 5 วันหลังจากเจาะเลือด
6) สิ่งส่งตรวจมีภาวะเม็ดเลือดแดงแตกหรือเลือดมีการแข็งตัวที่ชัดเจน
7) ใช้สารกันเลือดแข็งที่ไม่ใช่ชนิด EDTA
3.2. ดีเอ็นเอ
1) ข้อมูลที่ติดฉลากบนหลอดไม่สอดคล้องกับข้อมูลในเอกสารขอตรวจที่แนบมา ข้อมูลไม่สมบูรณ์ หรือข้อมูลไม่สามารถอ่านได้อย่างชัดเจน
2) ไม่มีเอกสารยินยอมการส่งตรวจ หรือ ข้อมูลไม่สมบูรณ์
3) หลอดเก็บดีเอ็นเอมีการปนเปื้อน รอยแตก ฝาปิดหลวม หรือสถานการณ์อื่น ๆ ที่อาจนำไปสู่การรั่วไหลของดีเอ็นเอ
4) ได้รับตัวอย่างที่ไม่ตรงตามเกณฑ์ที่กำหนด
5) ปริมาณดีเอ็นเอน้อยกว่าที่ต้องการ หรือมีการทำลายของสายดีเอ็นเอที่ชัดเจน
6) ส่งมาในอุณหภูมิไม่เหมาะสม
4. ระยะเวลารายงานผล
26 วันทำการหลังจากตัวอย่างถึงห้องปฏิบัติการ
5. ที่อยู่จัดส่งสิ่งส่งตรวจ
บริษัท แบงคอกจีโนมิกส์อินโนเวชั่น จำกัด (มหาชน)
เลขที่ 3689 ถนนพระราม 4 แขวงพระโขนง เขตคลองเตย กทม. 10110
การตรวจ Sentis™ ให้บริการโดย
บริษัท วัฒนา เมดิคอล แอนด์ เวลล์บีอิง จำกัด (HealthSmile)
Wattana Medical and Wellbeing Co., Ltd.
899/17 หมู่ 2 ต.บ้านคลองสวน อ.พระสมุทรเจดีย์ สมุทรปราการ 10290
ที่มา : SENTIS-05-V02_คู่มือการส่งตรวจ SENTIS HDC_v.1_16-01-2023
Update ล่าสุด 16 มค 2566


